文字サイズ
- 大
- 中
- 小


2025年現在、がんは依然として日本人の死因の第1位であり、年間約37万人ががんで亡くなっています。
統計(※1)によれば、日本人の2人に1人は一生のうちにがんにかかるとされており、がんはもはや特別な病気ではなく、だれにでも起こり得る「国民病」といえる存在です。
高齢化の進展に伴い、がんの罹患率は増加傾向にあり、早期発見・早期治療の重要性がますます高まっています。がんは、遺伝子の突然変異によって生じた異常な細胞(がん細胞)が制御不能な増殖を続けることで発症します。
正常な細胞は一定の寿命を持ち、役割を終えると自然に死滅しますが、がん細胞はこの仕組みが壊れており、無限に分裂・増殖し続けます。
がん細胞は周囲の組織に浸潤したり、血液やリンパの流れに乗って転移する性質を持ち、これが生命を脅かす大きな要因となります。 がんは医学的には「悪性腫瘍」と呼ばれ、これに対して、増殖はするものの転移せず、生命に直接影響を与えないものは「良性腫瘍」と分類されます。
2023年の統計(※2)によると、がんによる死亡の多くは以下の6つの部位に集中しています。
これらのがんは、定期的ながん検診によって早期に発見することが可能であり、治療成績の向上にもつながります。
がんの発症には、遺伝的要因だけではなく、生活習慣が大きく関与します。以下のような習慣ががんのリスクを高めることが知られています。
これらのリスクを減らすことで、がんの予防につながります。
また、近年では、がんゲノム医療や個別化医療の進展により、患者さんの遺伝情報に基づいた治療が可能となり、より効果的で副作用の少ない治療が期待されています。日本では、厚生労働省が策定した「がん対策推進基本計画」に基づき、がん検診受診率の向上、医療体制の整備、患者支援の充実など、総合的ながん対策が進められています。医療機関では、がん相談支援センターの設置や、緩和ケアの充実、若年層(AYA世代)への支援など、多様なニーズに応える体制が整えられつつあります。
※1 国立がん研究センター がんの統計2025
※2厚生労働省 2023年人口動態統計(確定数)の概況
がんは、単に一か所にとどまる病気ではありません。がん細胞は、自ら生存と増殖のために、体内を移動する力を持っています。 血液やリンパの流れを利用して体内の別の場所に移動する能力をもっています。この移動によって、がんが別の臓器に広がる現象を「転移」と呼びます。
がん細胞は、原発巣(最初にがんが発生した場所)から血液やリンパ管に侵入し、体内を循環することで、肺、肝臓、脳、骨などの血流が豊富な臓器に到達します。到達した先でがん細胞が定着し、再び増殖を始めることで新たながんの病巣(転移巣)が形成されます。転移は、がんの診断時にすでに見つかることもあれば、治療中や治療後に新たに発見されることもあります。つまり転移はがんの進行においていつでも起こり得る現象であり、予測が難しいのが特徴です。
転移と混同されやすい言葉に「浸潤(しんじゅん)」があります。
浸潤とは、がん細胞が液体が染み込むように、周囲の正常な組織に入り込んでいく状態を指します。浸潤はがんの局所的な広がりであり、転移は遠隔臓器への拡散という点で異なります。
がんの進行度は「ステージ分類(病期分類)」によって評価されます。
例えば、転移が確認された場合、がんはステージⅣ(4期)と診断されます。これは、がんが原発巣を超えて遠隔臓器に広がっている状態であり、進行がんと呼ばれます。 ただし、ステージⅣであっても、近年の医療技術の進歩により、治療によって長期生存や寛解が可能なケースも増えています。 特に「オリゴメタスタシス(限局転移)」と呼ばれる、転移が少数に限られている場合には、局所治療と全身療法の併用で治癒を目指すことも可能です。
がんの治療後に再びがんが現れることを「再発」といいます。 再発は、原発巣の近くで起こる「局所再発」、リンパ節などの「領域再発」、そして肺や肝臓など遠隔臓器で起こる「遠隔再発」に分類されます。 一方、がんの「完治」とは、手術などでがんを切除した後、5年間にわたって再発が認められない状態を指します。 これは医学的な目安であり、5年を過ぎても再発する可能性がゼロになるわけではありませんが、統計的には再発リスクが大きく低下するとされています。
がんの治療方針を決定するうえで最も重要な指標のひとつが「ステージ分類(病期分類)」です。
これは、がんがどの程度進行しているかを示すもので、ステージ0期からステージⅣ期までの5段階に分類されます。この分類は、がんの種類や部位によって多少異なりますが、基本的にはTNM分類という国際的な基準に基づいています。
これらの要素を組み合わせて、以下のようなステージに分類されます。
ステージ分類は、がんの進行度を客観的に評価するだけでなく、治療方針の決定、予後の予測、患者とのコミュニケーションにおいても非常に重要な役割を果たします。AIによる画像診断やがんゲノム解析の進歩により、より精密なステージ判定が可能となっており、患者さん一人ひとりに最適な治療が提供される時代が到来しています。
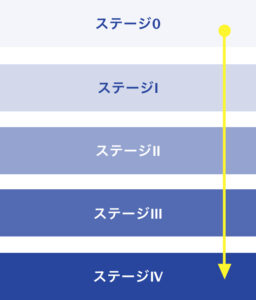
| ステージ0期(上皮内がん) |
がん細胞が粘膜の表層にとどまっており、まだ周囲の組織に浸潤していない状態です。 治療法:内視鏡的切除(EMR・ESD)など、身体への負担が少ない治療が中心。 |
|---|---|
| ステージⅠ期(早期がん) |
がんが粘膜下層や筋層まで浸潤しているものの、リンパ節や他の臓器への転移は認められない状態です。 治療法:外科手術やロボット支援手術など。臓器の機能を温存できる場合もあります。 |
| ステージⅡ期(局所進行がん) |
がんが周囲の組織に広がっているか、リンパ節への転移が一部認められる状態です。 治療法:外科手術に加え、補助的な化学療法や放射線療法を併用することが一般的です。 |
| ステージⅢ期(進行がん) |
がんが広範囲に浸潤し、複数のリンパ節への転移が確認される状態です。 治療法:手術、化学療法、放射線療法、免疫療法などを組み合わせた治療が行われます。 |
| ステージⅣ期(遠隔転移がん) |
がんが肺、肝臓、骨、脳などの遠隔臓器に転移している状態です。 治療法:免疫チェックポイント阻害薬、分子標的薬、ホルモン療法、CAR-T療法など、全身療法が中心。 |
肺がんは、現在も日本人のがん死亡原因の第1位であり、特に高齢者を中心に増加傾向が続いています。
肺がんは、肺そのものから発生する「原発性肺がん」と、その他の臓器で発生したがんが肺に転移してきた「転移性肺がん(肺転移)」に分けられます。
早期に発見されれば手術によって治癒が期待できるがんですが、発見時はすでに進行していることも多く、放射線治療、抗がん剤治療、免疫療法など組み合わせた治療が必要になるケースも少なくありません。
全身のがんの中でも、治療が難しいがんの一つとされています。
ⅠA期:がんの大きさは3cm以下で最も早期の段階。
ⅠB期:がんの大きさは3cmを超えるが、転移はない。
治療法:手術が第一選択。肺の一部を切除する「区域切除」や「葉切除」が行われます。
予後:5年生存率は80~90%以上と高く、早期発見が鍵です。
ⅡA期:がんの大きさは3cm以下でもリンパ節転移あり。
ⅡB期:がんの大きさは3cmを超え、リンパ節転移あり。
治療法:手術に加えて、再発予防のために補助化学療法が行われることが多いです。
予後:5年生存率は60〜70%程度。術前に抗がん剤を使う「術前化学療法」も検討されます。
ⅢA期:同じ側の縦隔(心臓や食道のある部分)や肺門リンパ節に転移。
ⅢB期:反対側の縦隔や首のつけ根のリンパ節に転移。
治療法:手術が難しい場合が多く、化学療法+放射線療法が中心。症例によっては手術も検討されます。
予後:5年生存率は30〜50%。治療の個別化が重要です。
IVA期:同じ肺の別の場所や胸膜、胸水にがん細胞がある。
IVB期:遠隔臓器に転移がある。
治療法:手術は行わず、免疫療法、分子標的薬、化学療法などの全身治療が中心です。
予後:5年生存率は10〜20%。ただし、転移が限られている場合には、放射線や手術を併用することで長期生存が期待できることもあります。
肺は、全身の血液が流れ込む臓器であり、毛細血管が非常に豊富です。このため、他の臓器で発生したがん細胞が血流に乗って肺に到達し、肺転移を起こしやすい構造になっています。
また、肺がんが他の臓器に転移した場合でも、治療は「肺がん」として行われます。これは、がんの性質は原発巣に依存するためであり、転移先の臓器に合わせた治療ではなく、肺がんに適した治療が選択されます。
肺がんは、早期発見であれば治癒が期待できる一方で、進行すると治療が複雑になり、長期的な管理が必要となるがんです。
AI診断、ゲノム解析、ロボット手術、重粒子線治療などの技術革新により、治療の選択肢と精度は大きく進化しています。
がんと診断されたとき、医師から提案される治療法は大きく分けて3つの標準治療と、近年注目されている第4の治療法があります。
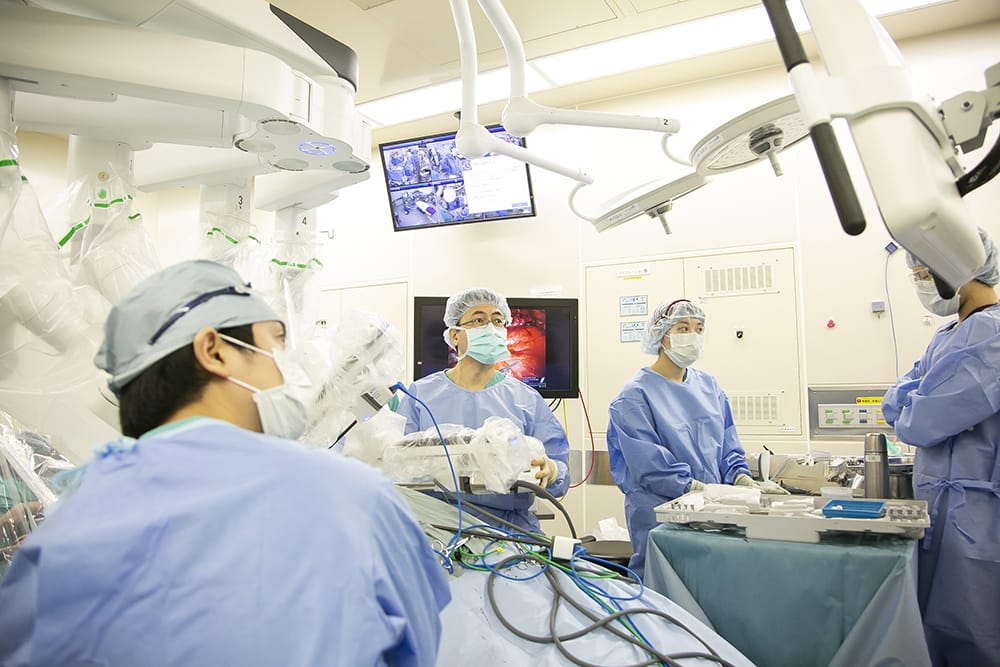
手術療法は、がん治療の中でも最も根治性が高い治療法のひとつです。
がんの病巣を直接切除することで、がん細胞を物理的に取り除くことができるため、早期がんに対しては特に有効です。
がんが発生した臓器だけでなく、周辺の組織やリンパ節に転移がある場合は、それらも含めて切除する「拡大手術」が行われることもあります。
手術の目的は、がんの完全切除と再発の予防です。
特徴:がんの根治を目指す治療法。早期発見されたがんに対しては、単独で完治が期待できます。
課題:身体への負担が大きく、術後の回復に時間がかかる場合があります。
臓器の一部を切除することで、機能障害が残る場合もあります。
手術支援ロボットの導入が全国のがん拠点病院を中心に進んでおり、身体への負担が少ない手術(低侵襲手術)として注目されています。
代表的なロボットには、「da Vinci Xi」と、「hinotori」があります。
腹部や胸部に数か所の小さな穴を開けるだけで手術が可能。傷口が小さく、術後の痛みも軽減。
精密な操作により、血管や神経を傷つけるリスクが低く、出血量が抑えられる。
入院期間が短く、社会復帰も早い。美容面でも優れている。
3D高精細画像で患部を10倍に拡大して確認でき、ロボットアームは人間の手以上の自由度を持つ関節構造で、繊細な動きが可能。
化学療法は、抗がん剤を用いてがん細胞の増殖を抑える治療法です。がん細胞は全身に広がる可能性があるため、化学療法は全身に作用する治療として、手術や放射線治療と並ぶ「がんの三大治療法」の一つに位置づけられています。
副作用を軽減する支持療法(制吐剤、造血因子製剤など)の進歩により、日常生活を維持しながら治療を続けることが可能になっています。
近年では、がん細胞の特定の性質(遺伝子変異やタンパク質)を狙い撃ちする分子標的薬や、ホルモンの働きを抑えるホルモン療法が登場し、副作用が少なく、より効果的な治療が可能になっています。
これらの薬剤は、がんゲノム検査によって適応が判断され、個別化医療(プレシジョン・メディシン)の中核を担っています。
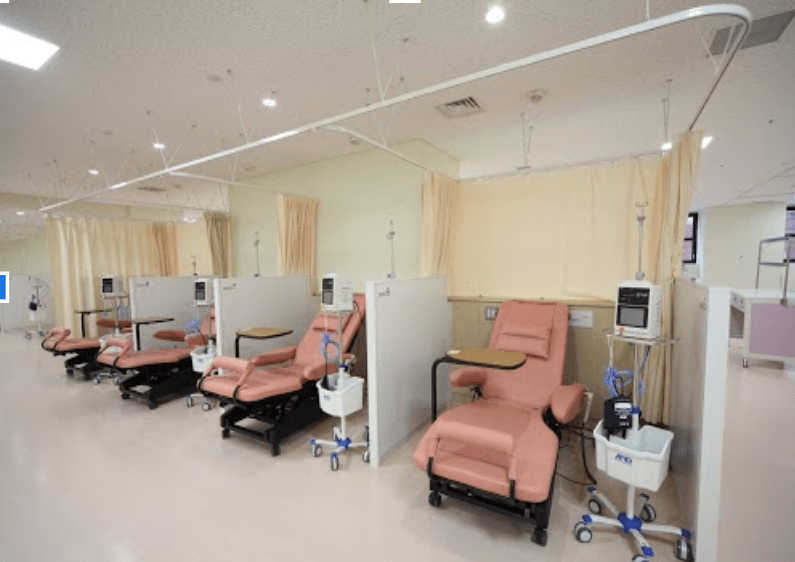
全国のがん拠点病院を中心に外来化学療法センターが整備され、通院しながら治療を受けるスタイルが主流となっています。
化学療法は、がん治療の中心的な役割を担いながら、より安全に、より生活に寄り添った形へと進化しています。
今後も、新薬の開発や個別化医療の進展により、さらに効果的で副作用の少ない治療が期待されています。
放射線治療は、がん細胞に高エネルギーの放射線を照射することで、細胞のDNAを損傷させ、増殖や分裂を抑制する治療法です。
手術を伴わない非侵襲的な治療であるため、身体への負担が少なく、特に高齢者や手術・薬物療法が困難な患者にも適用可能です。
放射線はがん細胞だけでなく、照射範囲内の正常な組織にも影響を及ぼす可能性があります。
そのため、治療計画は高度に個別化され、照射範囲・線量・角度などを厳密に管理します。
副作用の予防:皮膚炎、粘膜炎、倦怠感などの副作用を最小限に抑えるため、最新の画像誘導技術(IGRT)や強度変調放射線治療(IMRT)が活用されています。
生活支援:治療中の生活指導や栄養管理、心理的サポートも重要な要素です。
がん免疫療法は、私たちの体に本来備わっている「免疫」の力を活用して、がん細胞を攻撃・排除する治療法です。
免疫とは、細菌やウイルスなどの異物を認識し、排除する生体防御システムであり、がん免疫療法はこの仕組みを応用してがんに立ち向かいます。
従来の手術・放射線・抗がん剤治療に加え、「第4の治療選択肢」として注目されており、特に免疫機能が保たれている早期のがん患者に対しては、長期的な効果が期待されています。
免疫チェックポイント阻害薬(ICI)
がん細胞は、免疫細胞の攻撃を回避するために「免疫のブレーキ」となる分子(PD-1、PD-L1、CTLA-4など)を利用します。
免疫チェックポイント阻害薬はこのブレーキを解除し、T細胞の攻撃力を回復させることでがん細胞を排除します。
代表的な薬剤と適応がん種:
※副作用として、自己免疫疾患に似た症状(間質性肺炎、甲状腺機能障害など)が報告されています。
がん免疫療法は、1970年代のBCG療法などに始まり、現在では第5世代の治療法として、個別化医療や遺伝子解析技術と融合しながら進化を続けています。
特に、免疫チェックポイント阻害薬などは、治癒の可能性をもたらす治療法として世界的に注目されています。
がん免疫療法は、患者さん自身の免疫力を活かした治療法であり、長期的な効果と副作用の少なさが特徴です。
治療の選択肢として、他の療法と併用することで相乗効果が期待されるケースも多く、今後さらに普及が進むと考えられています。
ご自身やご家族が治療を検討される際には、医師と十分に相談し、最新の情報をもとに最適な治療法を選択することが重要です。